Nuestros servicios de investigación clínica
Estamos comprometidos con brindar una atención segura y de alta calidad a los pacientes que participan en nuestros protocolos clínicos. Para ello, contamos con instalaciones dedicadas y equipos especializados que acompañan cada etapa del estudio.

Hemos colaborado con más de 100 aliados en distintas áreas terapéuticas, entre ellas:
Nuestros investigadores cuentan con la experiencia y las credenciales necesarias para cumplir con estándares internacionales, garantizando estudios confiables y de alto rigor científico.
Colaboración estratégica de TecSalud con la industria farmacéutica
Trabajamos con compañías farmacéuticas de prestigio internacional, fortaleciendo nuestro compromiso con la innovación y el desarrollo de soluciones que transforman la salud.
Capacidades y Servicios
En TecSalud reunimos experiencia, infraestructura y procesos para colaborar de manera efectiva con la industria en investigación clínica.
Investigadores: Más de 30 médicos especialistas y líderes de opinión con experiencia en protocolos internacionales.
Especialidades: Cáncer, neurología, enfermedades infecciosas, gastroenterología, vacunas, entre otras.
Infraestructura: Áreas exclusivas para voluntarios, quirófanos, salas de infusión, laboratorios y espacios de monitoreo clínico.
Regulación y comités: Comités propios de Ética, Investigación y Bioseguridad, con tiempos de dictamen ágiles y cumplimiento normativo nacional e internacional.
Acompañamos a patrocinadores y voluntarios a lo largo de todo el ciclo del estudio clínico, desde la evaluación inicial hasta el cierre del protocolo.
Infraestructura de primer nivel
Cuidamos cada detalle para garantizar calidad y contamos con áreas hospitalarias que
complementan nuestros servicios.

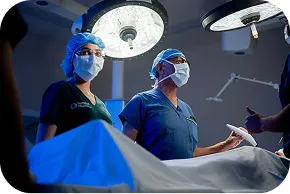
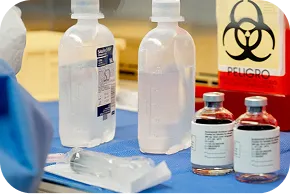
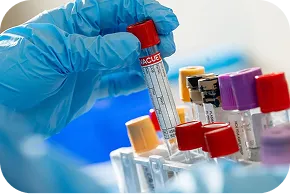



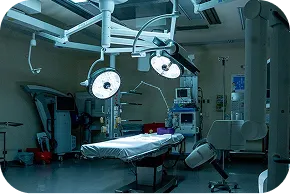



Investigadores e infraestructura de vanguardia
Nuestros investigadores cuentan con formación especializada y experiencia en estudios clínicos internacionales, garantizando calidad y confiabilidad en cada protocolo.
El Hospital Zambrano Hellión es un sitio de investigación clínica con más de 10 años de experiencia, respaldado por tecnología de vanguardia, programas integrales y centros especializados. Sus instalaciones ofrecen un entorno seguro, confortable y certificado para la atención médica e investigación clínica.
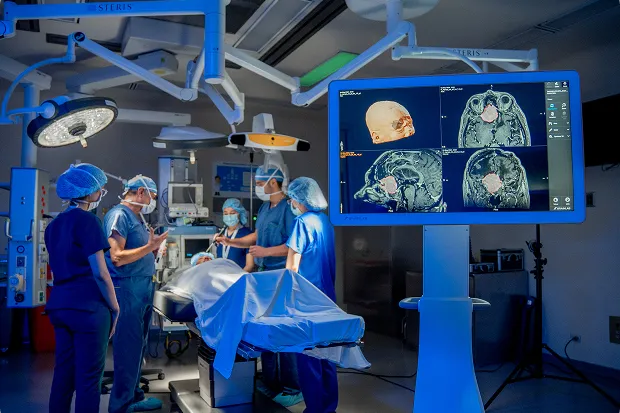
Calidad y confianza en cada estudio
Cumplimos con regulaciones nacionales e internacionales y garantizamos procesos éticos, transparentes y auditables en toda la investigación clínica.
En TecSalud estamos comprometidos a adherirnos a los requerimientos regulatorios para llevar a cabo cualquier estudio de investigación de acuerdo al Reglamento de la Ley General de Salud en Materia de Investigación para la Salud. También cumplimos con estándares de Buenas Practicas Clínicas y en proceso de certificación por el Programa de Investigación para la Protección de Humanos (HRPP).
Diseñamos estrategias de reclutamiento adaptadas a cada protocolo, en coordinación con su propio Investigador Principal. Colaboramos con instituciones públicas y especialistas externos para ampliar el acceso a pacientes, aprovechando nuestra ubicación estratégica y red de referencia.
Clasificación de riesgo para los protocolos
En TecSalud promovemos la transparencia y la ética en cada estudio clínico. De acuerdo con el Artículo 17 del Reglamento de la Ley General de Salud en Materia de Investigación para la Salud, los protocolos se clasifican según el nivel de riesgo para las personas participantes.
A continuación, puedes consultar las tres clasificaciones de riesgo y acceder a la documentación correspondiente para protocolos académicos y de la industria.

Sin riesgo
Corresponde a estudios en los que no se realiza ninguna intervención o modificación intencionada sobre las variables fisiológicas, psicológicas o sociales de los participantes.
Incluye, entre otros:
Riesgo mínimo
Incluye estudios en los que los procedimientos utilizados son similares a los que se realizan habitualmente en una consulta o estudio médico de rutina, y en los que el riesgo para las personas participantes es bajo.
Algunos ejemplos de este tipo de estudios son:
Estos estudios se realizan con seguimiento médico y están diseñados para minimizar cualquier molestia para el participante.


Riesgo mayor
Corresponde a estudios que incluyen procedimientos más complejos o tratamientos en evaluación, y que por su naturaleza requieren un control médico más estrecho y criterios de seguridad específicos.
En esta categoría se encuentran, por ejemplo:
Aunque estos estudios implican un mayor nivel de control y seguimiento, todos cuentan con la supervisión de equipos médicos especializados y comités de ética, que priorizan la seguridad, el bienestar y los derechos de las personas participantes en todo momento.
Etapas de la investigación clínica
Cuatro fases que permiten validar la seguridad, eficacia y continuidad de nuevos tratamientos:
Esta fase sirve para evaluar la seguridad y determinar la dosis adecuada de un nuevo tratamiento (medicamento, terapia, vacuna, etc.).
En esta fase se evalúa su eficacia y además de continuar evaluando la seguridad del tratamiento.
El objetivo de esta fase es confirmar la eficacia, monitorear efectos secundarios y comparar con tratamientos existentes.
En esta fase se monitorea a largo plazo la eficacia y seguridad después de la aprobación regulatoria.
¿Deseas participar en un protocolo de investigación en TecSalud?
Nuestro equipo acompaña el proceso de sometimiento ante los comités y la coordinación del estudio clínico.
Tiempo estimado de resolución interna: aproximadamente 2 meses (no incluye tiempos de respuesta del investigador, industria o autoridades sanitarias).

Comités de ética
Comprometidos con la integridad, la seguridad y los derechos de los participantes, nuestros comités garantizan el cumplimiento de principios éticos y normativos en cada estudio.

¿Tienes pacientes que puedan participar en estudios clínicos?
Únete a nuestro programa de referencia de pacientes y contribuye al avance de la investigación médica.
En TecSalud buscamos colaboradores internos y externos que deseen ofrecer a sus pacientes la posibilidad de participar en protocolos clínicos, siempre bajo criterios éticos, científicos y de seguridad.
Al referir a tus pacientes, les brindas la oportunidad de acceder a tratamientos innovadores y alternativas terapéuticas en evaluación, con el acompañamiento de un equipo médico especializado y una atención personalizada durante todo el proceso.
Si te interesa participar o conocer más sobre los protocolos disponibles, ponte en contacto con nosotros:
investclinica@servicios.tecsalud.mx
Teléfono: (81) 8888- 0000 ext. 3764



